SILICAN SILICON SYSTEMS SYSTEMS
PSHE இன் சிறப்பியல்புகள் 1. PSHE இல் நிலை. 1. PSHE இல் நிலை. 4 குழு, முகப்பு Subgroup, 4 குழு, முகப்பு Subgroup, 3 காலம் 3 வரிசை 3 காலம் 3 வரிசை 3 வரிசை AR \u003d 28 AR \u003d 28 டிகிரி ஆக்சிஜனேற்றம்: விஷத்தன்மை பட்டம்: -4, ஆக்சைடுகள்: ஆக்சைடுகள்: SIO (அலட்சியமாக) SIO (அலட்சியம்) SIO 2 (அமிலிக்) SIO 2 (அமிலத்திறன்) ஆசிட்-ஃபவுண்ட் அமிலம்-ஃப்ளவுண்ட் எச் 2 SIO 3 H 2 SIO 3
Z \u003d + 14 z \u003d p \u003d 14 +1 p \u003d 14 n \u003d 28-14 \u003d 14 n \u003d 28-14 \u003d 14 e \u003d 14 e \u003d 14 +14) 2) 8) 4 +14) 2) 8 ) S 2S 2P 3S 3P.

சிலிக்கான் மூன்றாவது (ஆக்ஸிஜன் மற்றும் ஹைட்ரஜன் பிறகு) மூன்றாவது (ஆக்ஸிஜன் மற்றும் ஹைட்ரஜன்) மூன்றாவது (ஆக்ஸிஜன் மற்றும் ஹைட்ரஜன் பிறகு) உறுப்பு பரவலாக உள்ளது: அதன் பங்கு ஒரு உறுப்பு பரவலாக இருக்க வேண்டும்: இது நிலப்பரப்பு பட்டை அணுக்களின் மொத்த எண்ணிக்கையில் 16.7% ஆகும். 16.7% பிராந்திய பட்டை அணுக்களின் மொத்த எண்ணிக்கையில். இயற்கையில், சிலிக்கான் சிலிக்கான் சிலிக்கிக் அமில டை ஆக்சைடுகளின் மற்றும் உப்புகள் (சிலிகேட்ஸ்) வடிவத்தில் மட்டுமே காணப்படுகிறது. அலுமினிய அலுமினியவர்கள் மிகவும் பரவலாக உள்ளனர். இயற்கையில், சிலிக்கான் சிலிக்கான் சிலிக்கிக் அமில டை ஆக்சைடுகளின் மற்றும் உப்புகள் (சிலிகேட்ஸ்) வடிவத்தில் மட்டுமே காணப்படுகிறது. அலுமினிய அலுமினியவர்கள் மிகவும் பரவலாக உள்ளனர்.

MAIN MAINS SILICON MAIN SILICON MAINDS al 2 O 3 * 2SIO 2 * 2H 2 O - வெள்ளை களிமண் Al 2 o 3 * 2sio 2 * 2h 2 o - வெள்ளை களிமண் K 2 O * Al 2 O 3 * SIO 2 - புலம் பிளம் கே 2 ஓ * அல் 2 ஓ 3 * SIO 2 - புலம் பிளம் கே 2 ஓ * அல் 2 ஓ 3 * 6SIO 2 * H 2 O - MICA K 2 O * AL 2 O 3 * 6SIO 2 * H 2 O - SIO 2 SIO 2 SIO 2 SIO 2 SIO 2 SIO 2 மணல் அல்லது நதி மணல்

சிலிக்கான் கனிமங்கள் மற்றும் பாறைகள் இராச்சியத்தில் முக்கிய உறுப்பு ஆகும். பெரும்பாலும், இது குவார்ட்ஸ் கனிமங்களின் வடிவத்தில் காணப்படுகிறது (யாருடைய வகைகள் - ஃப்ளைண்ட், சிலிக்கா (மணல்), நீலம், ஜாஸ்பர்) மற்றும் மலை படிக, (யாருடைய வகைகள் உள்ளன: ametyyst, smetyyst, புகைபிடித்த topaz). சிலிக்கான் கனிமங்கள் மற்றும் பாறைகள் இராச்சியத்தில் முக்கிய உறுப்பு ஆகும். பெரும்பாலும், இது குவார்ட்ஸ் கனிமங்களின் வடிவத்தில் காணப்படுகிறது (யாருடைய வகைகள் - ஃப்ளைண்ட், சிலிக்கா (மணல்), நீலம், ஜாஸ்பர்) மற்றும் மலை படிக, (யாருடைய வகைகள் உள்ளன: ametyyst, smetyyst, புகைபிடித்த topaz). அடிக்கடி, சிலிக்கான் கிட்டத்தட்ட காணப்படவில்லை. அடிக்கடி, சிலிக்கான் கிட்டத்தட்ட காணப்படவில்லை.

சில கடல் உயிரினங்கள் பெரிய அளவுகளில் சிலிக்கான் குவிக்கின்றன. சில கடல் உயிரினங்கள் பெரிய அளவுகளில் சிலிக்கான் குவிக்கின்றன. தங்கள் பணக்கார கடல் தாவரங்கள் ஆல்கா, விலங்குகள் இருந்து, சிலிக்கான் நிறைய adioles, சிலிக்கான் கடற்பாசிகள் உள்ளன. தங்கள் பணக்கார கடல் தாவரங்கள் ஆல்கா, விலங்குகள் இருந்து, சிலிக்கான் நிறைய adioles, சிலிக்கான் கடற்பாசிகள் உள்ளன.

ஏ தொழில்துறையில் - மின் உலைகளில் நிலக்கரி மறுசீரமைப்பு A. தொழில்துறையில் - மின்சார உலைகளில் நிலக்கரி குறைப்பு SIO 2 + 2C \u003d SI + 2CO SIO SIO 2 + 2C \u003d SI + 2CO b. ஆய்வகத்தில் - சிலிக்கா உலோகங்கள் குறைப்பு b. ஆய்வகத்தில் - சிலிக்கா 3SIO 2 + 4AL \u003d 3SI + 2AL 2 O 3 3SIO 2 + 4AL \u003d 3SI + 2AL 2 O 3

1) chelops silicon - பழுப்பு பவுடர் 1) remorphous silicon - பழுப்பு பவுடர் டி உருகும் 1420 சி. டி உருகும் 1420 பிபி. 2) படிக சிலிக்கான் - ஒரு பலவீனமான உலோக மினு கொண்ட திட, இருண்ட சாம்பல் நிறம், வெப்ப மற்றும் மின் கடத்துத்திறன் 2) படிக சிலிக்கான் உள்ளது - ஒரு பலவீனமான உலோக மினு கொண்ட திட, இருண்ட சாம்பல், வெப்பம் மற்றும் மின் கடத்துத்திறன் உள்ளது

ஒரு) சாதாரண பொருட்களுடன் தொடர்பு கொள்ளுங்கள். ஒரு) சாதாரண பொருட்களுடன் தொடர்பு கொள்ளுங்கள். எஸ்ஐ-குறைத்தல் முகவர் 1) Halogens 1) SI + 2F 2F 2F 2 \u003d SF 4 - SILIC FLOWORIDE SI + 2F 2F 2 \u003d SF 4 - சிலிக்கான் ஃவுளூரைடு 2) ஆக்ஸிஜன் 2 உடன்) ஆக்ஸிஜன் எஸ்ஐ + ஓ 2 சியோ 2 -OXYDE SILICON (LV) SI + O 2 SIO 2-SIO 2-Oxider Silicon (LV) 3) நைட்ரஜன் 3) நைட்ரஜன் 3SI + 2N 2 \u003d SI 3 N 4 சிலிக்கான் நைட்ரைடு 3SI + 2N 2 \u003d SI 3 N 4-NATIDE SILICON 4 ) கார்பன் 4 உடன்) கார்பன் Si + c \u003d sic-carry silicon அல்லது si + c \u003d sic-carbide சிலிக்கான் அல்லது கார்போர்ட் கார்பொரண்ட்

Si-oxidizer si-oxidizing முகவர் 5) உலோகங்கள் 5) உலோகங்கள் si + 2mg \u003d t mg 2mg \u003d t mg 2mg \u003d t mg 2 si-silicidic kuangium நேரடியாக சிலிக்கான் ஹைட்ரஜன் நேரடியாக பதில் இல்லை. நேரடியாக சிலிக்கான் ஹைட்ரஜன் எதிர்வினை இல்லை. SIH 4 மறைமுகமாக பெறப்படுகிறது. SIH 4 மறைமுகமாக பெறப்படுகிறது. MG 2 SI + 4HCL \u003d 2MGCL 2 + SIH 4 MG 2 SI + 4HCL \u003d 2MGCL \u003d 2MGCL 2 + SIH 4 (அமைதியான, விஷ வாயு) (அமைதியான, விஷ வாயு)

B) சிக்கலான பொருள்களுடன் தொடர்பு 1) HF 1 உடன் மட்டுமே HF 1 உடன் தொடர்பு கொள்ளுங்கள்) ஹாலோஜென் வளர்ப்பவர்கள் இருந்து எதிர்வினை HF SI + 4HF \u003d SIF 4 + 2 SI + 4HF \u003d SIF 4 + 2H 2 2) உடன் மட்டுமே கலவையாகும் நைட்ரிக் மற்றும் திரவ 2) அமிலங்கள் இருந்து. நைட்ரஜன் மற்றும் திரவ 3Si + 12HF + 4HNO 3 \u003d 3SIF 4 + 4NO + 8H 2 O 3SI + 12HF + 4HNO 3 \u003d 3SIF 4 + 4NO + 8H 2 O மற்ற அமிலங்களின் நடவடிக்கையின் கீழ் ஒரு அடர்ந்த ஆக்ஸைடு ஃபிலிம் சியோ 2 சிலிக்கான் மேற்பரப்பில் மற்ற அமிலங்களின் நடவடிக்கையின் கீழ் சிலிக்கான் மேற்பரப்பில் உருவாகிறது, ஒரு அடர்ந்த ஆக்ஸைடு ஃபிலிம் சியோ 2 3 உருவாக்கப்பட்டது) அல்கலி தொடர்பு 3) ஆல்கலி தொடர்பு H 2 O \u003d 2 SIO 3 + 2H 2 SI + 2NAOH + H 2 O \u003d NA 2 SIO 3 + 2H 2

திறப்பு. 1834 ஆம் ஆண்டில், ரஷ்ய வேதியியலாளர் கெட்ஸி ரஷியன் பெயரை இந்த உறுப்பு கொடுத்தார். 1834 ஆம் ஆண்டில், ரஷ்ய வேதியியலாளர் கெட்ஸி ரஷியன் பெயரை இந்த உறுப்பு கொடுத்தார். சிலிக்கான் 1825 ஆம் ஆண்டில் சிலிக்கான் திறக்கப்பட்டது, 1825 ஆம் ஆண்டில் ஸ்வீடிஷ் வேதியியலாளரான ஸ்வீடிஷ் வேதியியலாளர் பெர்செலியஸ் மூலம் அவர் திறக்கப்பட்டது. பெரெஸீலியஸ்.

பயன்பாடு செமிகண்டக்டர் பொருட்கள் மற்றும் உலோக கலவைகள் பெற நுட்பத்தில் பயன்படுத்தப்படுகிறது. கண்ணாடி மற்றும் சிமெண்ட் பெறுவதற்கு, உலோக ஐந்து வெட்டிகள் - வெட்டும் இயந்திரங்கள். இது செமிகண்டக்டர் பொருட்கள் மற்றும் உலோகக்கலவைகளைப் பெற தொழில்நுட்பத்தில் பயன்படுத்தப்படுகிறது. கண்ணாடி மற்றும் சிமெண்ட் பெறுவதற்கு, உலோக ஐந்து வெட்டிகள் - வெட்டும் இயந்திரங்கள்.

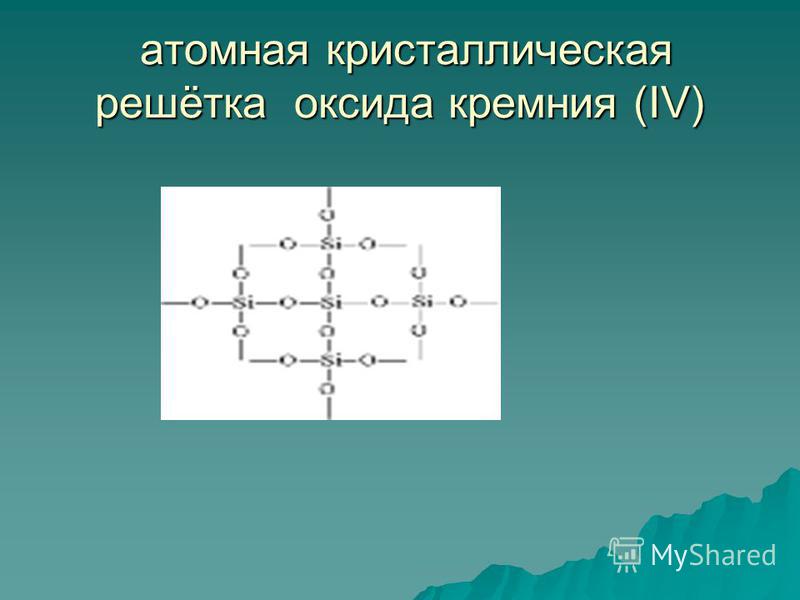
சிலிக்கான் ஆக்சைடு (iv) அல்லது சிலிக்கா சிலிக்கா (iv) அல்லது சிலிக்கா 1. கட்டிடம்: சிலிக்கான் ஆக்சைடு (IV) எந்த மூலக்கூறு (IV) எந்த மூலக்கூறு (கார்பன் டை ஆக்சைடு போன்றவை) இல்லை கார்பன் டை ஆக்சைடு), மற்றும் அணு தசை டை ஆக்சைடு) மற்றும் அணு கிரகந்திர லேடிஸ் SIO 2 திட மற்றும் reftcatory பொருள், எனவே திரவ தவிர, நீர் மற்றும் அமிலங்கள் கரைக்க முடியாது என்று, திரவ தவிர (halogeneous hydrochlic அமிலங்கள் நினைவில்). இது பேக்கிங் தவிர, நீர் மற்றும் அமிலங்களில் கலைக்கப்படவில்லை (ஆலசன் இனப்பெருக்கம் அமிலங்களை நினைவில் கொள்ளுங்கள்).




வேதியியல் ஆசிரியர்: Malinovskaya ஜூலியா Vladislavna.
தலைப்பில் ஒரு சுருக்கமான பாடம்: "கார்பன் மற்றும் சிலிக்கானின் நிலைப்பாடு, இரசாயன கூறுகளின் ஒரு குறிப்பிட்ட நேரத்தில், இந்த கூறுகளின் ஒப்பீட்டு பண்புகள். கார்பன் அலம்பாபி. "
வர்க்கம்: தரம் 9.
நோக்கம்: அணிவகுப்பு மற்றும் அணுக்களின் கட்டமைப்பின் மீது மாணவர்களின் அறிவை அமைப்பதற்கான நிலைமைகளை உருவாக்குதல், அமைப்பின் உறவு - கட்டமைப்பு - பொருட்களின் பண்புகள்
பணிகள்:
கல்வி:
பொதுமக்களின் அமைப்பில் உள்ள நிலைப்பாட்டைப் பொறுத்து அணுக்களின் கட்டமைப்பின் மீது மாணவர்களின் திறனாய்வு மற்றும் ஆழமடைதல் அறிவு; கலவை உறவு கட்டமைப்பு - அல்ட்ரோபிக் கார்பன் மாற்றங்களின் உதாரணத்தில் உள்ள பொருட்களின் பண்புகள்
மாணவர்களின் பொது அமைப்பின் விரிவாக்கம்
ஆராய்வதற்கான திறன்களை ஆய்வு செய்தல், ஒப்பிட்டு, முடிவுகளை எடுக்க, உறவுகளை நிறுவுதல்
கலவை, கட்டமைப்பு, பொருட்களின் பண்புகள் ஆகியவற்றின் உறவுகளின் கருத்தியல் யோசனையை வெளிப்படுத்துதல்; ஒரு புத்திசாலித்தனமாக வளர்ந்த ஆளுமையின் கல்வி; கலாச்சாரத்தின் கலாச்சாரத்தின் கல்வி
↑ வகை பாடம்: தற்செயலான இலக்கின் படி - அறிவின் முன்னேற்றம் மற்றும் பயன்பாடு; நிறுவனத்தின் முறையின் படி - அறிவு மற்றும் புதிய பொருட்களுடன் அறிவைப் பயன்படுத்துதல்
பயன்படுத்தப்படும் கல்வி தொழில்நுட்பங்கள்:
தகவல்
தனிப்பட்ட அனுபவம் தொழில்நுட்பம்
புலனுணர்வு அடையாள அபிவிருத்திக்கான நோக்குநிலை தொழில்நுட்பம்
வடிவம்: உரையாடல், சுதந்திர நடவடிக்கைகள்
உபகரணங்கள்: கணினி, ப்ரொஜெக்டர், கம்ப்யூட்டர் வழங்கல், சேகரிப்பு: "நிலக்கரி வகைகள்", வைர மற்றும் கிராஃபைட் படிக அணுகளின் மாதிரிகள்.
^ 1 நிலை பாடம்
நிறுவன. பாடம் தலைப்புகள் அறிவிப்பு.
வணக்கம்! இன்று பாடம் நாம் இரண்டு இரசாயன கூறுகள் பற்றி பேசுவோம்.
இந்த கூறுகளின் பெயர்கள் லத்தீன் வார்த்தைகளிலிருந்து "கார்போ" மற்றும் "Lyapis Sremyns" ஆகியவற்றிலிருந்து வருகிறது. (மாணவர்கள் உடனடியாக கார்பன் மற்றும் சிலிக்கான் பற்றி இருக்கும் என்று புரிந்து கொள்ளுங்கள்.).
"கார்போ" - "கார்போ" - "நிலக்கரி" - கார்பன், மற்றும் "Lyapis Sremyns" என்பது தீ - சிலிக்கான் என்று ஒரு கல் ஆகும்.
இன்று பாடம் நாம் முன்னர் பெற்ற அறிவைப் பயன்படுத்தி இந்த கூறுகளின் ஒப்பீட்டு பண்பு கொடுக்க வேண்டும்.
குறிப்பேடுகள், மாணவர்கள் பாடம் பொருள் எழுத: " ஒப்பீட்டு பண்புகள் கார்பன் மற்றும் சிலிக்கான் கூறுகள். "
ஒப்பிட்டு, இது அனைத்து முதல் தேர்வு, வரையறைகள் ஒப்பீடு. தயவுசெய்து என்னிடம் சொல், தயவுசெய்து, உங்கள் கருத்தில் என்ன அளவுகோல்கள், ஒப்பிட வேண்டும். மாணவர்கள் பதிலளிக்கிறார்கள்: PS இல் நிலை, அணுக்களின் கட்டமைப்பு, மதிப்பு, ஆக்ஸிஜனேற்றம் மற்றும் போன்ற அமைப்பு.
^ 2 நிலை பாடம்
அணுக்களின் கட்டமைப்பின் அறிவைப் பயன்படுத்தி, சோசலிஸ்ட் கட்சியின் நிலைப்பாட்டின் குணாம்சங்கள், மாணவர்கள் தங்களை தங்களை நிரப்புகிறார்கள் ஒப்பீட்டு அட்டவணை № 1.
அட்டவணை # 1. கார்பன் மற்றும் சிலிக்கான் கூறுகளின் ஒப்பீட்டு பண்புகள்
| ^ ஒப்பீடு ஒப்பீடு | இருந்து கார்பன் | Si. சிலிக்கன் |
| PS இல் நிலை. | 2 காலம், IV குழு, முதன்மை subgroup (a) | 3 காலம், IV குழு, முதன்மை subgroup (a) |
| கட்டிடம் அணுக்கள் | Z i \u003d + 6, p \u003d 6, e \u003d 6, n \u003d 12-6 \u003d 6, வெளிப்புற e \u003d 4 | Z i \u003d + 14, p \u003d 14, e \u003d 14, n \u003d 28-14 \u003d 14, வெளிப்புற e \u003d 4 |
| அணுக்களின் மின்னணு கட்டமைப்பு | 1s 2 2s 2 2p 2. | 1S 2 2S 2 2P 6 3S 2 3P 2 |
| மதிப்பு வாய்ப்புகள் | II ஒரு நிலையான நிலையில் IV ஒரு உற்சாகமான நிலையில் |
|
| ஆக்ஸிஜனேற்றத்தின் சாத்தியமான டிகிரி | -4 முதல் +4 வரை சி 4, சி 2 எச் 6, சி 2N 4, CAC 2, C, சி 2 எஃப் 2, CO, C 2 F 6, CO 2 | -4, 0, +2, +4 Mg 2 si, si, sio, sio 2 |
| ஆரம் அணு | அதிகரிக்கிறது |
|
| மின்சாரம் (உண்மையான அளவில்) | 2,5 | 1,9 |
| உயர் ஆக்சைடு, அதன் பாத்திரம், பெயரின் சூத்திரம் | CO 2 - அமிலம், கார்பன் மோனாக்சைடு (iv), கார்பன் டை ஆக்சைடு, கார்பன் டை ஆக்சைடு | SIO 2 - அமிலம், சிலிக்கான் ஆக்சைடு (IV) |
| அதிக ஹைட்ராக்சைடு, அதன் பாத்திரம், பெயரின் சூத்திரம் | H 2 CO 3 - பலவீனமான நிலையற்ற அமிலம் (CO 2 + H 2 O), உப்புகள் - கார்பனேட்ஸ் | H 2 SIO 3 பலவீனமான அமிலம், ஒரு பாலிமர் அமைப்பு உள்ளது (SIO 2 NH 2 O), உப்புகள் - சில்கேட்ஸ் |
| ஹைட்ரஜன் இணைப்பு | சி 4 - மீத்தேன் | பாவம் 4 - சிலான் (நிலையற்ற) |
| இயற்கையில் | கரிம பொருட்கள் தேவையான உறுப்பு | பூமியின் மேலோட்டத்தின் மிக பொதுவான (ஆக்ஸிஜன் பிறகு) உறுப்பு |
மேஜை நிரப்புவதில் சுயாதீன வேலை முடிவில், ஆசிரியர் குழுவில் குழுவில் எழுதப்பட்ட முன்கூட்டியே நிரப்புங்கள். கூட்டு நிரப்பலின் செயல்பாட்டில், ஆசிரியர்களுடன் சேர்ந்து மாணவர்கள் கொண்டாடுகிறார்கள், அவர்கள் கவனம் செலுத்த வேண்டிய அவசியமான கூறுகளின் சில அம்சங்களை உச்சரிக்கிறார்கள்:
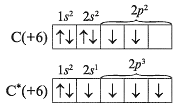
கிட்டத்தட்ட அனைத்து அதன் சேர்மங்கள், கார்பன் மற்றும் சிலிக்கான் tetravalent உள்ளன, i.e. கூறுகளின் தரவு அணுக்கள் உற்சாகமான நிலையில் உள்ளன. ஆசிரியர் (மாணவர்) குழுவில் அது காட்டுகிறது:
இருப்பு காரணமாக கார்பன் அணுக்களில் பல ஆக்ஸிஜனேற்ற டிகிரி கரிம கலவைகள், அதன் மிகவும் சொற்பொருள் டிகிரி ஆக்ஸிஜனேற்றத்தின் கனிம பொருட்களில்: -4, 0, +2, +4
கார்பன் மற்றும் சிலிக்கானில் உள்ள பண்பு வேறுபாடு சங்கிலி உருவாவதற்கு கார்பன் திறன் ஆகும். கார்பன் அணுக்கள், ஒருவருக்கொருவர் இணைக்கும், நிலையான கலவைகள், ஒத்த சிலிக்கான் கலவைகள் நிலையற்றவை.
^ 3 நிலை பாடம்
இரசாயன கூறுகளின் பண்புகள் - எளிய பொருட்களுக்கு.
ஒரு கணினி வழங்கல் வேலை.
கார்பன் அணுக்களுக்கு, Alleotropy வகைப்படுத்தப்படுகிறது. மாணவர்கள் கருத்து வரையறை வரையறை - "Allhotropy". ஆசிரியர் கேட்கிறார்: "முன்பு என்ன மூடிய இரசாயன கூறுகள் ஒதுக்கீடு மாற்றங்கள் உள்ளன?".
மாணவர்கள் எடுத்துக்காட்டுகள்: ஆக்ஸிஜன் உறுப்பு (ஓ) - ஓ 2 - ஆக்ஸிஜன், ஓ 3 - ஓசோன்; SERA உறுப்பு (கள்) - படிக மற்றும் பிளாஸ்டிக் சல்பர்.
மேலும், ஆசிரியர் மாணவர்களை கேட்கிறார், ஆல்டோ கார்பன் மாற்றங்களை அவர்கள் அறியலாம்.
கார்பன் பின்வரும் எளிய பொருட்கள் வடிவத்தில் உள்ளது: வைரம், கிராஃபைட், கார்பின்கள், fullerene. நிலக்கரி, சோட் கிராஃபைட் வகைகளாக கருதப்படுகிறது.
ஆர்வம் கரி.
அவருடன், மற்றொரு பழமையான நபர் நன்கு அறிந்திருந்தார்: அவர் நதியின் நடுவில் அவரை கண்டுபிடித்தார், நெருப்பின் பின்னால் இருந்தார். கரி ஒரு பெரிய போரோசிட்டி மற்றும் மூழ்கிவிடாது. 1785 ஆம் ஆண்டில், ஒரு விஞ்ஞானி - திவாய் லோவிட்ஸின் ஒரு வேதியியலாளர் ஒயின் அமிலம் (அசுத்தங்கள் காரணமாக பழுப்பு நிறத்தை) நிலக்கரி கலவையில் கலவையாகக் கொட்டினார். Lovitz தெளிக்கப்பட்ட தீர்வு கூடியிருந்தது, நிலக்கரியில் மணல் இருந்து வடிகட்டிய. வடிகட்டியில் ஒரு நிறமற்ற பொருள் உள்ளது. நிலக்கரி சித்திரவதைகளில் உள்ள அசுத்தங்களை உறிஞ்சிவிடும் என்று அது மாறியது. எனவே ஒரு திறந்த நிகழ்வு இருந்தது, இது Abodsion என்று அழைக்கப்படுகிறது.
பரப்புதல் - நிலக்கரி மற்றும் மற்றவர்களின் பண்புகள் திடப்படி அதன் மேற்பரப்பில் கேஸை வைத்திருங்கள். பொருட்கள், எந்த Aboardsion ஏற்படுகிறது மேற்பரப்பில், Adsorbents என்று அழைக்கப்படுகிறது.
நிலக்கரி ஆபிரிசிஷன் அவரது போரோசால் ஏற்படுகிறது. மேலும் துளைகள், நிலக்கரியின் மிகச்சிறந்த திறன். ஆனால், பொதுவாக, நிலக்கரி துளைகள் பல்வேறு பொருட்களுடன் நிரப்பப்படுகின்றன. அவற்றை சுத்திகரிக்க, நிலக்கரி நீர் நீராவி ஜெட் உள்ள சூடாக உள்ளது. இத்தகைய நிலக்கரி, உரிக்கப்படுகின்ற துளைகளுடன், செயல்படுத்தப்படுகிறது.
முதல் உலக போர்காம்பாட் விஷம் பொருட்களுக்கு எதிரான போராட்டத்தில் Adsocraption இன் நிகழ்வு பயன்படுத்தப்பட்டது. குளோரின் (மூச்சுத்திணறல் வாயு) 1915 இல் பயன்படுத்தப்பட்டது மேற்கு முன் ஆங்கிலேய-பிரெஞ்சு துருப்புக்களுக்கு எதிராக IPRA நகரத்திற்கு அருகில். தாக்குதல் குளோரின் ஒரு முழு பிரிவுக்கு (15 ஆயிரம் பேர் முடக்கப்பட்டனர், 5 ஆயிரம் பேர் இறந்துவிட்டனர்).
ரஷியன் பேராசிரியர் நிகோலே Zelinsky (பின்னர் கல்வி) ஜூலை 1915 காஸ் ஒரு சோதனை கண்டுபிடிக்கப்பட்டது மற்றும் ஒரு சோதனை நடத்தப்பட்டது, Adsorption நிகழ்வு அடிப்படையில் செயல்படும்.
சிலிக்கான் ஒரு எளிய பொருளை உருவாக்குகிறது - படிக சிலிக்கான். பவுடர் - பவுடர் சிலிக்கான் உள்ளது வெள்ளை நிறம்.
அடுத்து, ஆசிரியர் ஒவ்வொருவருக்கும் உடல் பண்புகளைத் தடுக்கிறது மற்றும் குறிக்கிறது எளிய பொருள்கார்பன் அணுக்கள் (ஸ்லைடுகள்) உருவாக்கப்பட்டது.
டயமண்ட் மற்றும் கிராஃபைட் கார்பன் அணுக்கள் கொண்ட வைர மற்றும் கிராஃபைட் போன்ற பல்வேறு உடல் பண்புகளை கொண்டுள்ளது என்ற உண்மையை மாணவர்களின் கவனத்தை ஈர்க்கிறது. ஏன்? (மாணவர்கள் எப்போதும் இந்த கேள்விக்கு பதிலளிக்க முடியாது). ஆசிரியர் டயமண்ட் மற்றும் கிராஃபைட் கிரிஸ்டிக் லீமின் பல்வேறு கட்டமைப்பிற்கு கவனம் செலுத்துகிறார்.
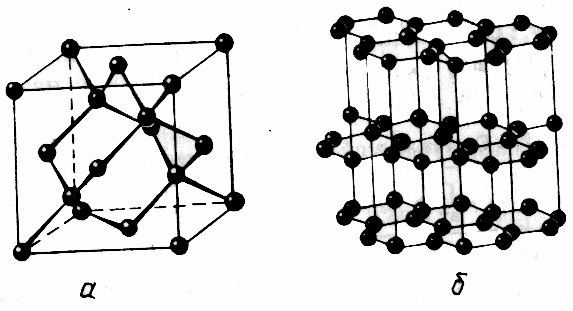
வைர படிகத்தில், ஒவ்வொரு கார்பன் அணுக்களும் நான்கு வலுவான கூட்டுறவு பத்திரங்களை உருவாக்குகின்றன, அவை TETRAHEDRON இன் டாப்ஸிற்கு அனுப்பப்படுகின்றன, அணுக்களுக்கு இடையில் உள்ள அனைத்து தொலைவுகளும் ஒரே மாதிரியானவை. கிராஃபைட்டில், அடுக்குகளில் உள்ள அணுக்களுக்கு இடையில் உள்ள தொலைவு அடுக்குகளுக்கு இடையில் உள்ள தூரம் (படிக சொற்களின் மாதிரிகள்) இடையேயான தூரம் விட மிகவும் சிறியதாகும்.
^ 4 நிலை பாடம்
அவரது குறிக்கோள்: மாணவர்களின் பொது அமைப்பின் விரிவாக்கம், வரலாற்றுடன் வேதியியல் சிகிச்சைமுறை நிறுவப்பட்டது.
முந்தைய பாடம், என வீட்டு பாடம், ஆசிரியர் கண்டுபிடிக்க மாணவர்கள் வழங்கினார் சுவாரஸ்யமான உண்மைகள் வைரத்தின் வரலாறு பற்றி மற்றும் ஒரு கணினி வழங்கல் ஒரு செயல்திறனை தயார் செய்யவும்.
பணி முடிந்த மாணவர்கள் இருந்தால், ஆசிரியர் அவற்றை வார்த்தையுடன் வழங்கவில்லை என்றால், அவர் கூறுகிறார், பின்னர் அவர் கூறுகிறார் மற்றும் அவரது விளக்கக்காட்சியை காட்டுகிறார்.
^ 5 மேடை பாடம்
சுருக்கமாக. பிரதிபலிப்பு.
மாணவர்கள் கேள்விகளுக்கு பதில்:
பாடம் என்ன புதிய கருத்துக்கள் ஆய்வு?
என்ன கேள்விகள் சிரமங்களை ஏற்படுத்தியது? முதலியன
பாடம் பாடத்திட்டத்தில் நல்ல மற்றும் சிறந்த அறிவைக் காட்டிய அந்த மாணவர்களின் மதிப்பீட்டை ஆசிரியர் செயலில் உள்ளனர்.
நூலகம்
லெவின் ஏ.என். பொது மற்றும் கனிம வேதியியல்: பரீட்சைக்கான பொருட்கள். - SPB.: "PAITITY", 2003 - 240 ப.
MALINOVSKAYA YU.V. வேதியியல். 6 வது வகுப்பு / புரோமேடிக் பாடநெறி. - SPB.: ICAR கூட 2002, - 76 ப.
Taube P. R. Rudenko E. I. ஹைட்ரஜன் இருந்து Nobelia வரை? - m.: Gosdo. வெளியிட உயர்நிலை பள்ளி", 1961 - 330 பக்.
வேதியியல்: 9 செல்கள் ஒரு பாடநூல். uch. / rudzitis g.e., ஃபெல்ட்மேன் F.G. - 11 வது எட். Pere. - எம்: ஞானம், 2010.
வரிசை எண் 14 ஆகும், கோர் +14, கோர் +14, கோர் - 14, எலக்ட்ரான்கள் - 14. காலம் III இன் காலம் - 14 எலக்ட்ரான்கள் மூன்று ஆற்றல் மட்டங்களிலும் நகர்த்தப்படுகின்றன. குழு IV இன் எண்ணிக்கை - வெளிப்புற ஆற்றல் மட்டத்தில் 4 எலக்ட்ரான்கள் ஆகும். அணுவின் ஆரம் கார்பன் விட அதிகமாக உள்ளது - எலக்ட்ரான்களை அதிகரிக்கும் திறன் அதிகரிக்கிறது. உலோகம் மற்றும் மறுவாழ்வு பண்புகள் அதிகரிப்பு (கார்பனுடன் ஒப்பிடுகையில்). Si ge sn pb. பொது பண்புகள் காலக்கெடு காலக்கட்டத்தில் உள்ள நிலையில் உள்ள சிலிக்கான். சி
படம் 2 விளக்கக்காட்சியில் இருந்து "சிலிக்கான்" தலைப்பு "சிலிகான்" என்ற தலைப்பில் வேதியியல் பாடங்கள்பரிமாணங்கள்: 960 x 720 பிக்சல்கள், வடிவம்: JPG. வேதியியல் பாடம் ஒரு படத்தை பதிவிறக்க, வலது சுட்டி பொத்தானை படத்தை கிளிக் செய்து "படத்தை சேமிக்கவும் ..." என்பதைக் கிளிக் செய்யவும். வகுப்பறையில் படங்களை காட்ட நீங்கள் ZIP காப்பகத்தில் அனைத்து படங்களையும் முற்றிலும் "சிலிக்கான் .ppt .ppt" விளக்கக்காட்சியை பதிவிறக்க முடியும். காப்பக அளவு 562 kb ஆகும்.
விளக்கக்காட்சி பதிவிறக்கசிலிக்கன்
"சிலிக்கான் பாடம்" - கார்பன் டை ஆக்சைடு தன்னை மற்றும் மனிதகுலத்தை பற்றி. ஜோடிகள் வேலை, பரஸ்பர சோதனை - பிழைகள் இல்லை (5), இரண்டு பிழைகள்- (4), முதலியன 3% காற்று - தலைச்சுற்று, காதுகளில் சத்தம், தூக்கம். 20% - ஒரு நபர் எல்லாம். உலோக அல்லாத மற்றும் உலோக பண்புகள் வெளிப்பாடு மீது. கட்டளை மதிப்பீடு. கார்பன் இருந்து radii அணுக்களின் அளவு பற்றி என்ன சொல்ல முடியும்?
"சிலிக்கான் மற்றும் அதன் சேர்மங்கள்" - இயற்கை சிலிக்கான் கலவைகள் கருத்தில் கொள்ள. சிலிக்கானின் ஒட்டுமொத்த பண்புக்கூறு கூறுகளை கொடுங்கள். சிலிக்கான் பெறுதல். சிலிக்கான் முதல் 1811 ஆம் ஆண்டில் கே Lyssak மற்றும் டெர்ரா மூலம் கண்டுபிடிக்கப்பட்டது. அணுக்களின் கட்டமைப்பு மற்றும் பண்புகள். சிலிக்கான் ஆக்சைடு, கார்பன் ஆக்சைடு (IV) மாறாக, தண்ணீரில் தொடர்பு கொள்ளாது. குறைக்கடத்தி. Tplant (si) \u003d 1415? சி, டப்ளவ் (டயமண்ட்) \u003d 3730? சி
"சிலிக்கான் ஐசோடோப்புகள்" - பால்கிரிஸ்டல்லின் சிலிக்கான் பெறுதல். அணு வெகுஜனத்திலிருந்து சிக்கலான சிதறலின் குழுவின் அதிகபட்ச நிலைப்பாட்டின் சார்பு. பர்னர். ஒரு படிக விதை உருவாக்குதல். ஜோனோ சுத்திகரிக்கப்பட்ட சிலிக்கான். பாதுகாப்பு உள்ளடக்கம். ஐசோடோப்பு-செறிவூட்டப்பட்ட சிலிகான் -80 இன் வெப்ப கடத்துத்திறன். வளரும் ஒற்றை படிகங்கள். விதைகளின் நீளத்தின் மூலம் ஐசோடோப்புகளின் செறிவு விநியோகம்.
"சிலிக்கான் கலவைகள்" - பல்வேறு குவார்ட்ஸ். ஜஸ்பர். சிலிகேட்ஸ் பெறுதல். இயற்கை சிலிக்குகள். சிலிக்கான் ஆக்சைடு. SIO2 அடிப்படையில் கனிமங்கள். இரசாயன பண்புகள் SIO2. சிலிக்கான் திறப்பு. சிலிக்கான் மற்றும் அதன் இணைப்புகள். சிலிக்கான். Agate. ஆக்ஸிஜனேற்றத்தின் அளவு. மின்னணு கட்டமைப்பு. சிலிகேட்ஸ் மற்றும் ஹைட்ரஜன். Rhinestone. இயற்கையில் கண்டுபிடித்து. சிசிலன்.
"கார்பன் மற்றும் சிலிக்கான்" - இரசாயன பண்புகள். மிகவும் மிதமான திடப்பொருள்களில் ஒன்று. சைலிக் பிரிக்ஸ். இந்த கலவையை ஜெனரேட்டர் எரிவாயு என்று அழைக்கப்படுகிறது. வைர லத்தியின் Fig.1 மாதிரி. இதன் விளைவாக எரிவாயு இலவச நைட்ரஜன் மற்றும் கார்பன் ஆக்சைடு (II) ஆகியவற்றைக் கொண்டுள்ளது. வளிமண்டலத்தில் 99% க்கும் மேற்பட்ட கார்பன் கார்பன் டை ஆக்சைடு வடிவில் கொண்டுள்ளது. PSHE இல் நிலை.
"சிலிக்கான்" - சிலிக்கான் தோற்றத்தின் முடிவை வரை போதுமானதாக இல்லை 4 எலக்ட்ரான்கள். சிலிக்கான் ஆக்சைடு (iv). காலகான் ஒட்டுமொத்த சிறப்பியல்பு காலத்தில் காலக்கட்டத்தில் உள்ள நிலையில் உள்ளது. சிலிக்கான் ஆய்வகங்களில், SIO2 சிலிக்கான் ஆக்சைடு மீட்டமைப்பது. உடல் பண்புகள். சிலிக்காட்கள் - சிலிக்கிக் அமிலத்தின் உப்புக்கள். சிலிக்கேட் தொழில்.
மொத்தம் 6 விளக்கக்காட்சிகளில் மொத்தம்
சிலிக்கான் பூமியின் மேலோட்டத்தின் ஒரு முக்கிய அம்சமாகும், இது ஆக்ஸிஜன் (சுமார் 27.6%) பிறகு இரண்டாவது இடத்தில் உள்ளது.
சிலிக்கான் மூன்று ஐசோடோப்புகள் உள்ளன: நான் (92.27%); (4.68%); (3.05%).
சிலிக்கான் இரண்டு Alleotropic மாற்றங்களில் உள்ளது: உறுதியான மற்றும் கிரிஸ்டல். கட்டமைப்பில் உள்ள வேறுபாடு இந்த மாற்றங்களின் இயல்பான பண்புகளில் வேறுபாட்டை நிர்ணயிக்கிறது. இறுக்கமான சிலிக்கான் - பழுப்பு பவுடர், ஒரு குறிப்பிட்ட உருகும் புள்ளி இல்லை. படிக சிலிக்கான் தோற்றம் இது ஒரு உலோக கிளிட்டர், referactory (1400 ° C இன் உருகும் புள்ளி) ஒரு உலோக, இருண்ட சாம்பல் போல தோன்றுகிறது, ஆனால் அது உலோகங்களுக்கு காரணம் அல்ல, அது பலவீனமாக இருப்பதால், அது சற்றே மின்சாரம் மற்றும் வெளிப்பாடுகளை ஏற்படுத்துகிறது இரசாயன பண்புகள் அல்லாத உலோகங்கள்.
அமைப்பு படிக சிலிக்கான் வைரத்தின் கட்டமைப்பைப் போலவே. அதன் படிகத்தில், ஒவ்வொரு அணுவும் நான்கு பிற கூட்டு பத்திரங்களுடன் இணைக்கப்பட்டுள்ளது. மேலும், சிலிக்கான் அணுக்களுக்கு இடையிலான கூட்டு பிணைப்பு டயமண்டில் கார்பன் அணுக்களுக்கு இடையில் விட பலவீனமாக உள்ளது. சாதாரண நிலைமைகளின் கீழ் கூட, சில இணைப்புகள் அழிக்கப்பட்டன மற்றும் இலவச எலக்ட்ரான்கள் தோன்றும், இது ஒரு சிறிய மின் கடத்துத்திறனை ஏற்படுத்தும். சூடான மற்றும் வெளிச்சம் போது, \u200b\u200bஅழிவு பத்திரங்களின் எண்ணிக்கை அதிகரிக்கிறது, எனவே, மேலும் இலவச எலக்ட்ரான்கள் தோன்றும், மின் கடத்துத்திறன் அதிகரிக்கிறது.
கிரிஸ்டல் சிலிக்கான் - செமிகண்டக்டர். குறைக்கடத்திகள் அழைப்புகள் மற்றும் மின்காப்புப் பத்திரங்களின் கடத்துத்திறன் இடையே ஒரு இடைநிலை இடத்தை ஆக்கிரமித்துள்ள பொருள்களை அழைக்கின்றன. மேலும் விவரம் நீங்கள் உயர்நிலை பள்ளியில் இயற்பியல் படிப்பினைகளில் இந்த நிகழ்வு படிப்பீர்கள். இந்த சொத்துக்களில், சிலிக்கான் பயன்பாடு ஏசி திருத்திகள் மற்றும் சூரிய பேனல்கள் உற்பத்தியை அடிப்படையாகக் கொண்டது, சூரியனின் வெப்ப ஆற்றலை மின்சாரமாக மாற்றும். இத்தகைய பேட்டரிகள் பூமியின் செயற்கை செயற்கைக்கோள்களில் நிறுவப்பட்டுள்ளன, நிலப்பரப்பு நிலைமைகளில் பயன்படுத்தப்படுகின்றன.
சிலிக்கான் இதர அமைப்பு (வரைபட மற்றும் படிக) பல்வேறு இரசாயன செயல்பாடுகளை பல்வேறு இரசாயன செயல்பாடு தீர்மானிக்கிறது. சாதாரண நிலைமைகளின் கீழ், படிக சிலிகான் ஃப்ளோரைனில் உள்ள மிருதுவான, மற்றும் உறுதியான தீக்காயங்கள்:

சிலிக்கான் சூடான போது, \u200b\u200bஅது பல அல்லாத உலோகங்கள் (ஆக்ஸிஜன், குளோரின், நைட்ரஜன், கார்பன், சாம்பல்), மற்றும் அது உயர்த்தி ஒரு பெரிய எண் சூடான. சிலிக்கான் உலோகங்கள் இணைக்கிறது. இந்த கலவைகள் சைடிக் என்று அழைக்கப்படுகின்றன.
பணி. பணி 1. தொடர்புடைய எதிர்வினை சமன்பாடுகளை எழுதவும் மற்றும் ஆக்சிஜனேற்ற எதிர்வினைகளில் சிலிக்கான் செயல்பாடுகளை குறிப்பிடவும்.
பணி 2. மெக்னீசியம், அலுமினியத்துடன் இரசாயன சிலிகான் எதிர்வினைகளின் சமன்பாடுகளை எழுதுங்கள். ஆக்ஸிஜனரை குறிப்பிடவும், முகவரை குறைத்தல். ஆக்சிஜனேற்றத்தின் பட்டம் சிலிக்கான் வெளிப்படுத்துகிறது.
அமிலங்கள் (திரவ எ.கா. தவிர) சிலிக்கான் மீது செயல்படாது, எனினும், சிலிக்கானுடனான ஆல்காலி மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல் மெட்டல்.
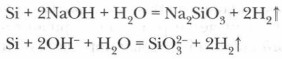
உயர் வெப்பநிலையில், சிலிக்கான் தங்கள் ஆக்சைடுகளிலிருந்து பல உலோகங்களை மீட்டெடுக்கிறது:
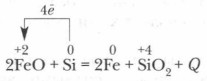
அதன் தூய வடிவத்தில், சிலிக்கான் இயற்கையில் காணப்படவில்லை.
முதல் முறையாக, சிலிக்கான் 1822 ஆம் ஆண்டில் ஸ்வீடிஷ் விஞ்ஞானி I. பெரெஸீலியஸ் சிலிக்கான் ஃவுளூரைடு SIF 4 மெட்டல் பொட்டாசியம் 400 ° C க்கு வெப்பமடைகிறது. இது சியோ 2 மெட்டல் மெட்டல் மெம்னீசியம் மீண்டும் பெற எளிதானது.
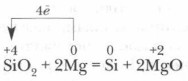
சிலிக்கான் துறையில், மணல் மற்றும் கோக் கலவையை சூடான போது பொதுவாக பெறப்படுகிறது:
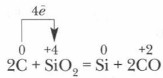
மீட்கப்பட்ட சிலிக்கான் ஓரளவு அதிகமாக கார்பன், மற்றும் வடிவங்களுடன் செயல்படுகிறது காபெருடம் கார்போரண்ட் ஒரு வைர-போன்ற படிகமான லேட்டீஸ் உள்ளது, அது மிகவும் நீடித்திருக்கும், எனவே கடினத்தன்மை மீது, அது வைரத்திற்கு நெருக்கமாக உள்ளது, அரைக்கும் கற்கள் மற்றும் அரைக்கும் வட்டங்கள் உற்பத்தி பயன்படுத்தப்படுகிறது.
பணி. SIC - சிலிக்கான் கார்பைடு அல்லது கார்பன் சிங்கோசைட்டை எப்படி சரிசெய்வது? நியாயமான பதிலை கொடுங்கள்.
சிலிக்கான் கலவை
இயற்கையில், சிலிக்கான் முக்கியமாக சிலிக்கா (மணல்) சியோ 2 மற்றும் சிலிக்காட்கள் வடிவத்தில் உள்ளது. சுத்தமான சிலிகான் ஆக்சைடு படிகங்கள் (IV) பல பாலிமர்ஃபிக் மாற்றங்களை உருவாக்குகின்றன, இதில் ஒரு சுரங்க படிக வடிவில் காணப்படும் குவார்ட்ஸில் ஒன்று. அழகாக நிற குவார்ட்ஸ் படிகங்கள் (செவ்வாய், புகைபிடிக்கும் டாப்ஸ், பிளாக் தார்மன், கார்னிதியன், அகேட், ஓபல், ஜாஸ்பர், முதலியன) அரை விலைமதிப்பற்ற கற்கள்.
சிலிக்கான் ஆக்சைடு (iv) SIO 2 ஒரு திடமான பயனற்ற பொருள் (உருகும் புள்ளி 1713 ° C), தண்ணீரில் கரையக்கூடியது (படம் 54). அவர் வைத்திருக்கிறார் அணு கிரிஸ்துவர் லேடிஸ் (படம் 55): எந்த மூலக்கூறுகள் உள்ளன, ஒவ்வொரு சிலிக்கான் அணு அருகில் நான்கு ஆக்ஸிஜன் அணுக்கள் உள்ளன - ஒரு விசித்திரமான ஸ்பேடியல் சட்ட. ஒரு குவார்ட்ஸ் துண்டு ஒரு பெரிய மூலக்கூறு போல. குவார்ட்ஸ் ஒரு கனிம பாலிமர், அதன் சூத்திரம் (SIO 2) n ஆகும்.
இங்கே நீங்கள் தலைப்பில் ஒரு பாடம் பதிவிறக்க முடியும்: "கார்பன் மற்றும் சிலிக்கான் நிலை இரசாயன கூறுகள் ஒரு காலக்கெடு நிலை, அவர்களின் அணுவின் கட்டமைப்பு. கார்பன், allotropic மாற்றங்கள்" பொருள்: வேதியியல்: வேதியியல். இந்த ஆவணம் பாடம் ஒரு நல்ல மற்றும் உயர்தர பொருள் தயார் செய்ய உதவும்.
தேதி _____________ வகுப்பு _______________
பொருள்:கார்பன் மற்றும் சிலிக்கான் ஆகியவை இரசாயன கூறுகளின் காலக்கட்டத்தில், அவற்றின் அணுக்களின் கட்டமைப்பு. கார்பன், அலோராபிக் மாற்றங்கள்.
| அணு கட்டமைப்பின் திட்டம் | கடைசி ஆற்றல் மட்டத்தின் மின்னணு அமைப்பு | உயர் ஆக்ஸைடு சூத்திரம்RO. 2 | கொந்தளிப்பான சூத்திரம் ஹைட்ரஜன் இணைப்பு RH. 4 | |
| 1. கார்பன் | சி+6) 2 ) 4 | …2 எஸ். 2 2 பி 2 | சி +4 ஓ 2 | சி -4 எச். 4 |
| 2. சிலிக்கான் | Si. +14) 2 ) 8 ) 4 | …3 எஸ். 2 3 பி 2 | Si. +4 ஓ 2 | Si. -4 எச். 4 |
இந்த உறுப்புகளின் வெளிப்புற எரிசக்தி மட்டத்தில் 4 எலக்ட்ரான்கள் உள்ளன, எனவே, கார்பன் மற்றும் சிலிக்கான் ஆக்சிஜனேற்றம் +4 மற்றும் -4 ஆகியவற்றைக் காட்டுகின்றன.
இந்த திட்டத்தில் இருந்து கார்பன் தொகுதி வெளிப்புற மட்டத்தில் இரண்டு unpaired எலக்ட்ரான்கள் உள்ளன என்று காணலாம் (சிலிக்கான் போன்றவை). இது கார்பன் மற்றும் சிலிக்கான் ஆக்சிஜனேற்றம் +2 (உதாரணமாக, CO - கார்பன் மோனாக்சைடு) ஒரு பட்டம் பெற முடியும் என்று விளக்குகிறது. ஒரு உற்சாகமான நிலைக்கு திருப்புதல், S- எலக்ட்ரான்களில் ஒன்று ஒரு இலவச p-inrbital க்கு செல்லலாம். பின்னர் 4 unpaired எலக்ட்ரான்கள் மற்றும் விஷத்தன்மை அளவு +4 மற்றும் - 4 தோன்றும் தோன்றும்.
2. ஒரு subgroup உள்ள பண்புகள் மாறும்
கட்டுப்பாட்டு எண்ணின் அதிகரிப்புடன் கார்பன் ஒரு துணை குழுவில், அணு அணுக்கரு கட்டணம் அதிகரிக்கிறது, வெளிப்புற மட்டத்தில் உள்ள எலக்ட்ரான்களின் எண்ணிக்கை தொடர்ந்து வருகிறது, அணுக்கள் உள்ள ஆற்றல் மட்டங்களின் எண்ணிக்கை வளர்ந்து வருகிறது மற்றும் கார்பனிலிருந்து அணுவின் ஆரம் அதிகரிக்கிறது நேர்மறை மையத்திற்கு எதிர்மறையான எலக்ட்ரான்களின் ஈர்ப்பு பலவீனமடைகிறது மற்றும் எலக்ட்ரான்களை அதிகரிக்கக்கூடிய திறனை அதிகரிக்கிறது, இதன் விளைவாக, கார்பன் ஒரு subgroup இல் வரிசை எண் அதிகரிப்பு, அல்லாத உலோக பண்புகள் குறைந்து, மற்றும் உலோக மேம்பட்டது.
சி மற்றும் எஸ்ஐ - அல்லாத உலோகங்கள், GE - செமிகண்டக்டர், SN மற்றும் PB - உலோகங்கள்.
கார்பன். Altyrpopy கார்பன்
கார்பன் இயற்கையில் காணப்படுகிறது , இலவச வடிவம் மற்றும் இணைப்புகளில் இருவரும். வெள்ளம் வடிவத்தில் காணப்படுகிறது alleotropic மாற்றங்கள் - டயமண்ட், கிராஃபைட், கார்பின், fullerene.
வைரம்
படிக பொருள், வெளிப்படையான, வலுவாக ஒளி கதிர்கள், மிகவும் கடினமாக உள்ளது, மிகவும் கடினமாக உள்ளது, ஒரு மின்சார தற்போதைய நடத்த முடியாது, அது வெப்ப வெப்பம் இல்லை, ρ \u003d 3.5 g / cm 3; T ° pl. \u003d 3730 ° C; T ° KIP. \u003d 4830 ° C.
P\u003e 50 ஆயிரம் ஏ.டி.யில் கிராஃபைட் இருந்து பெற முடியும்; T ° \u003d 1200 ° C.
விண்ணப்பம்:
வெட்டி பிறகு தூள், போர்கள், கண்ணாடி வெட்டிகள் அரைக்கும் - வைரங்கள்.
கிராஃபைட்
படிக பொருள், லேமினேட், ஒளிபுகா, இருண்ட சாம்பல், ஒரு உலோக மினு, மென்மையானது, மின்சார மின்னோட்டத்தை நடத்துகிறது; ρ \u003d 2.5 கிராம் / செ.மீ. 3.
விண்ணப்பம்:
அணு உலைகளில் நியூட்ரான் ரெட்டாரெர் எலெக்ட்ரோக்கள், பென்சில்கள், சில லூப்ரிகண்டுகளின் ஒரு பகுதியாகும்.
கர்பின்
கருப்பு தூள்; ρ \u003d 2 g / cm 3; குறைக்கடத்தி.
நேரியல் சங்கிலிகள் -C≡C-C≡C- மற்றும் \u003d c \u003d c \u003d c \u003d c \u003d கொண்டிருக்கிறது.
வெடிக்கும் போது சூடான தொடங்கும் போது.
பாடம்

